Aktivearre koalstof (AC) ferwiist nei de heechkoalstofhoudende materialen mei hege porositeit en sorpsjefermogen produsearre út it hout, kokosnootskillen, stienkoal en kegels, ensfh. AC is ien fan 'e faak brûkte adsorbinten dy't brûkt wurde yn ferskate yndustryen foar it fuortheljen fan ferskate fersmoargjende stoffen út wetter en loft. Om't AC synthetisearre wurdt út 'e lânbou- en ôffalprodukten, is it in geweldich alternatyf bliken te wêzen foar de tradisjoneel brûkte net-duorsume en djoere boarnen. Foar de tarieding fan AC wurde twa basisprosessen brûkt, karbonisaasje en aktivearring. Yn it earste proses wurde foargongers ûnderwurpen oan hege temperatueren, tusken 400 en 850 °C, om alle flechtige komponinten te ferdriuwen. Hege ferhege temperatuer ferwideret alle net-koalstofkomponinten út 'e foargonger lykas wetterstof, soerstof en stikstof yn 'e foarm fan gassen en teer. Dit proses produseart koalstof mei in hege koalstofynhâld, mar in leech oerflak en porositeit. De twadde stap omfettet lykwols de aktivearring fan earder synthetisearre koalstof. Fergrutting fan poargrutte tidens it aktivearringsproses kin yn trije kategoryen wurde: iepening fan earder ûnberikbere poaren, ûntwikkeling fan nije poaren troch selektive aktivearring, en ferbreding fan besteande poaren.
Gewoanlik wurde twa oanpakken, fysyk en gemysk, brûkt foar aktivearring om it winske oerflak en porositeit te krijen. Fysyk aktivearring omfettet de aktivearring fan karbonisearre koalstof mei oksidearjende gassen lykas loft, koalstofdiokside en stoom by hege temperatueren (tusken 650 en 900 °C). Koalstofdiokside wurdt meastentiids foarkar jûn fanwegen syn suvere aard, maklike ôfhanneling en kontrolearbere aktivearringsproses om 800 °C hinne. Hege poareuniformiteit kin wurde krigen mei koalstofdiokside-aktivearring yn ferliking mei stoom. Foar fysyk aktivearring wurdt stoom lykwols folle foarkar jûn boppe koalstofdiokside, om't AC mei in relatyf grut oerflak produsearre wurde kin. Fanwegen de lytsere molekulegrutte fan wetter fynt de diffúzje binnen de struktuer fan koalstof effisjint plak. Aktivearring troch stoom is fûn om sawat twa oant trije kear heger te wêzen as koalstofdiokside mei deselde mjitte fan konverzje.
In gemyske oanpak omfettet lykwols it mingen fan in foargonger mei aktivearjende aginten (NaOH, KOH, en FeCl3, ensfh.). Dizze aktivearjende aginten fungearje as oksidanten en ek as ûntwetteringsmiddels. Yn dizze oanpak wurde karbonisaasje en aktivearring tagelyk útfierd by in relatyf legere temperatuer fan 300-500 °C yn ferliking mei de fysike oanpak. As gefolch dêrfan beynfloedet it de pyrolytyske ûntbining en resulteart it dan yn útwreiding fan in ferbettere poreuze struktuer en in hege koalstofopbringst. De wichtichste foardielen fan in gemyske oanpak boppe in fysike oanpak binne de lege temperatuereasken, hege mikroporositeitsstrukturen, in grut oerflak en in minimalisearre reaksjetiid.
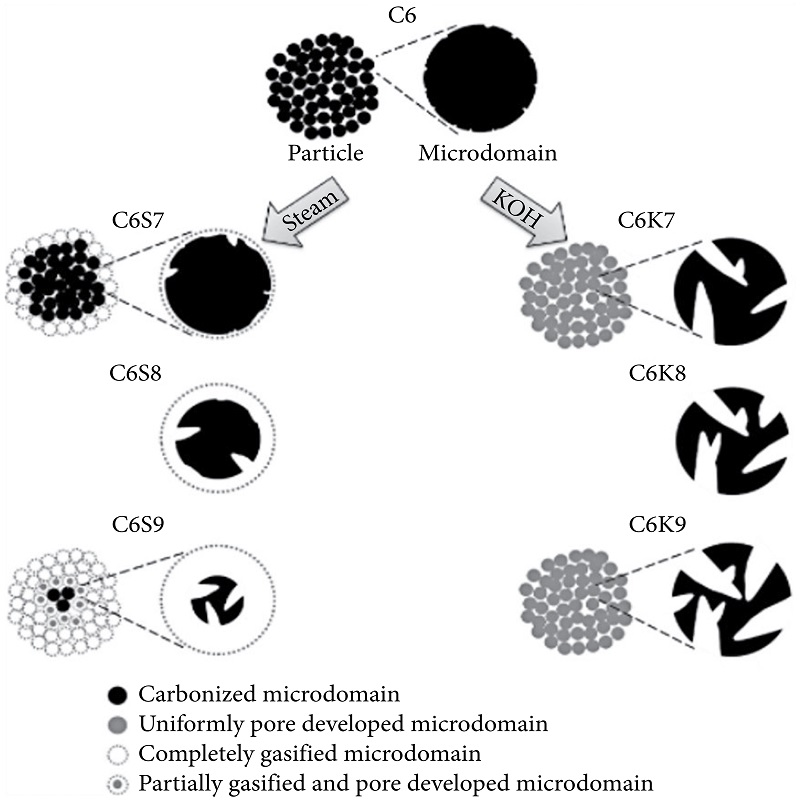
De superioriteit fan 'e gemyske aktivearringsmetoade kin ferklearre wurde op basis fan in model foarsteld troch Kim en syn meiwurkers [1] neffens hokker ferskate sferyske mikrodomeinen dy't ferantwurdlik binne foar de foarming fan mikropoaren fûn wurde yn 'e AC. Oan 'e oare kant wurde mesopoaren ûntwikkele yn 'e yntermikrodomeinregio's. Eksperiminteel foarmen se aktivearre koalstof út fenol-basearre hars troch gemyske (mei KOH) en fysike (mei stoom) aktivearring (figuer 1). Resultaten lieten sjen dat AC synthetisearre troch KOH-aktivearring in hege oerflakte hie fan 2878 m2/g yn ferliking mei 2213 m2/g troch stoomaktivearring. Derneist waarden oare faktoaren lykas poargrutte, oerflakte, mikropoarvolume en gemiddelde poarbreedte allegear better fûn yn KOH-aktivearre omstannichheden yn ferliking mei stoomaktivearre.
Ferskillen tusken AC taret út stoomaktivaasje (C6S9) en KOH-aktivaasje (C6K9), respektivelik, útlein yn termen fan mikrostruktuermodel.
Ofhinklik fan 'e dieltsjegrutte en de metoade fan tarieding kin it wurde yndield yn trije soarten: oandreaune AC, granulêre AC en kraal-AC. Oandreaune AC wurdt foarme út fyn granulearre ...
Pleatsingstiid: 18 juny 2022

